Modular Membrane Cell Electrolysers
Learn how chlorine and hydrogen are produced from brine in a modern and efficient membrane cell electrolyser.

Membrancellselektrolysörer har en förseglad modul som består av två kamrar, åtskilda av ett flexibelt katjonbytarmembran, för att förhindra att klor- och vätgaser blandas. De två kamrarna bildas av anod- respektive katodpansemblerna, och när de väl är anslutna till en elförsörjning är det där elektrolysen äger rum.
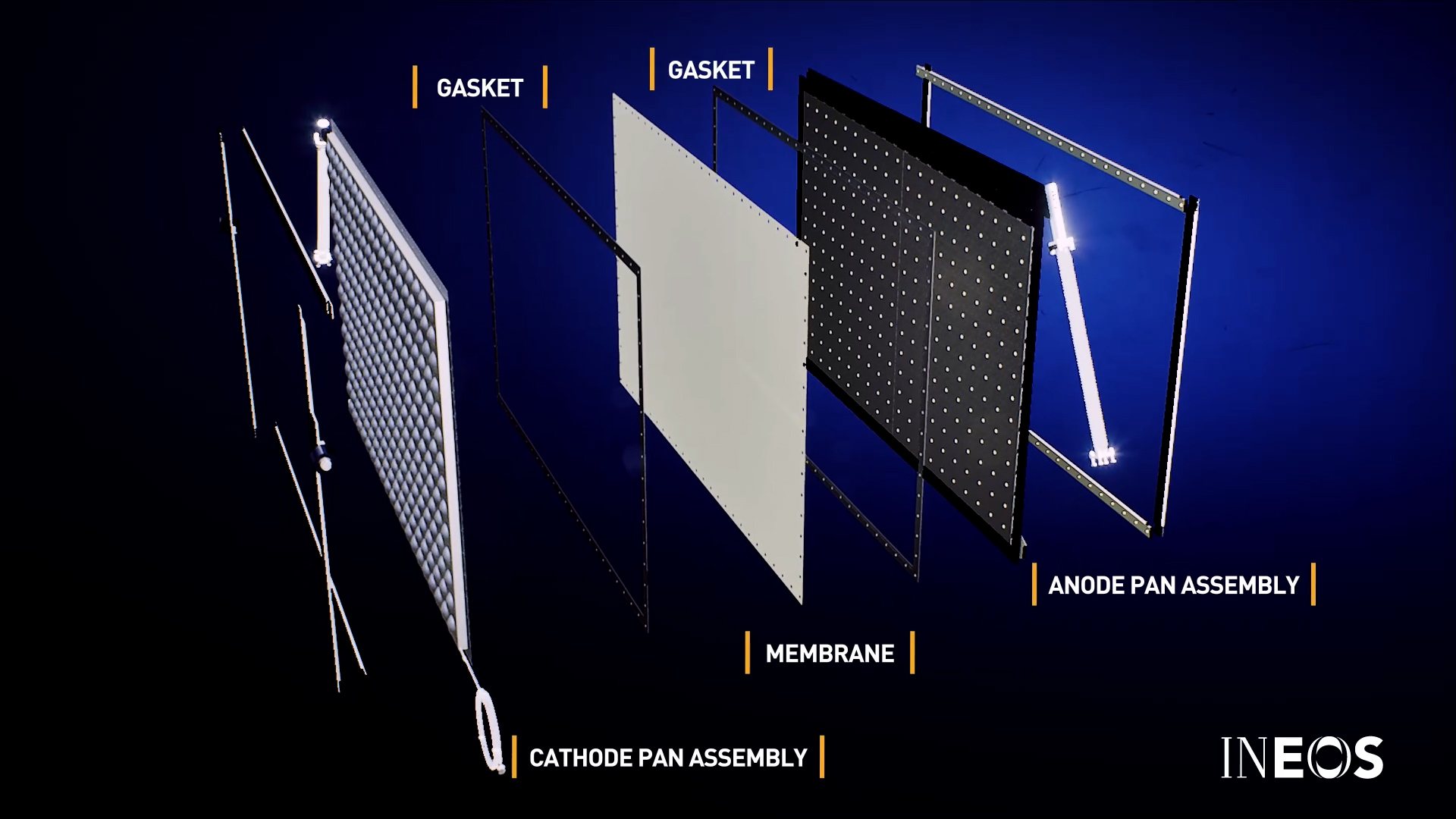
Anod- och katodaggregaten (elektroder) är kritiska designegenskaper hos en elektrolysör och måste tillverkas av speciella material för att förhindra korrosion av kloret.
Anoden är där kloret genereras och tillverkades historiskt av grafit- eller platinalegeringar. Moderna elektrolysörer har anoder tillverkade av titan för korrosionsbeständighet. Katodelementet är vanligtvis mindre känsligt för korrosion och tillverkas ofta av nickel, även om rostfritt stål kan användas.
Dessutom är varje elektrod belagd för att förbättra elektrolysprocessens effektprestanda och effektivitet.
- Katodpannbeläggningar elektrokatalytisktfrämjar H2-utveckling och ger motstånd mot föroreningsförgiftning och omvända strömmar vid avstängning.
- Anodpannbeläggningar är för den elektrokatalytiska främjandet av Cl2-evolution och har överlägsen alkalislitageprestanda och lägre utgångssaltlösningsvärden
Det flexibla membranet i mitten av varje modul stöds fullt ut i en "nollgapskonstruktion" för att förhindra klaffning eller klämning av membranmaterialet (tvärsnitt av en modulenhet som beskrivs nedan).

En modulär elektrolysör i industriell skala, såsom INEOS BICHLOR Electrolyser, består av sådana moduler som är elektriskt serielagda inom en ram. Vanligtvis installeras ett antal elektrolysörer i ett cellrum sida vid sida, med den mängd som är utformad för att möta anläggningens totala önskade kapacitet.

Operation
- Elektrolyt (saltlösning till anoderna och kaustisk till katoderna) kommer in genom matningsrör, helt vätande membranet i mitten av cellen, för i sig säkrare drift:

- Elektrisk ström börjar strömma genom elektrolyscellens metallspindlar och elektroder

- Natriumjoner (Na+) eller kaliumjoner (K+) passerar genom det halvgenomsläppliga jonbytarmembranet

- Klorgasbubblor bildas vid anoden och stiger till toppen av kammaren.
Vätgasbubblor bildas vid katoden och stiger till toppen

- Klor- och vätgaser extraheras sedan från toppen av sina respektive kamrar
Den totala reaktionen för elektrolys av saltlösning är: 2NaCl + 2H2O → Cl2 +H2+ 2NaOH